公司是国内药物安全评价行业龙头,根据Frost&Sullivan 报告,2019 年国内市场份额高达 15.7%,未来将继续受益于药物安评业务的外包需求,主要原因包括:1)药物安全评价 业务的外包率很高,将受益于新药研发的需求:很多中小型药企缺乏安评业务所需的符 合优良实验室规范(GLP)的实验室,因此安评外包的刚性需求很大。2)公司是国内少 数同时拥有中国、美国、经合组织(OECD)颁发的优良实验室规范(GLP 认证)的企业 之一,能满足全球客户需求。3)强大产能确保订单快速兑现:公司临床实验室面积处于 国内领先地位,实验动物种类齐全,强大产能确保订单迅速兑现。
全方位一站式服务能力将不断提升,海外业务将加速扩张
公司临床前与临床后业务的服务能力将同时提升,一站式服务能力将不断加强。公司原 来以临床前阶段的药物安评业务为主,但近年来药代动力学及药理与药效学的订单迅速 增加,临床试验产能也在扩张,一站式服务能力将不断提升。公司原来以中国客户为 主,2019 年收购美国Biomere 后海外订单迅速增加,估计2021 年上半年海外订单同比增 加近七成。Biomere 在北美客户基础坚实,公司实验动物及工程师资源丰富, 双方合作 将达成双赢效果,“昭衍”品牌在北美的市场认可度将越来越高。
业绩能见度很高,未来3 年将维持快速增长
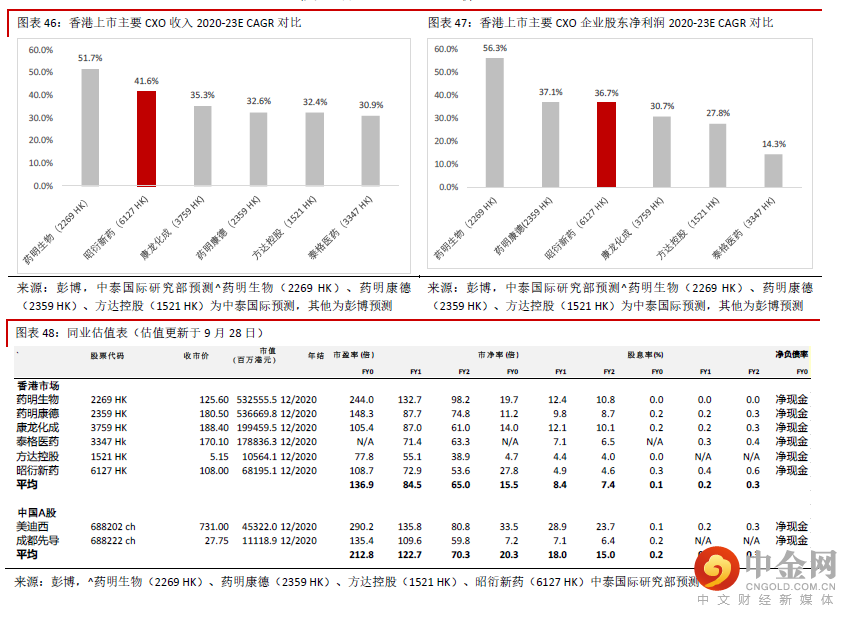
公司业绩能见度很高,预计总收入2020-23E CAGR 为41.6%,理由包括:1)公司2020 年 获得的约17 亿元新增订单中多数将于2021 年兑现。2)公司获取订单能力越来越强, 2021 年上半年新增订单约13 亿元,保守预计全年将获23 亿订单,未来也将快速增长。3)一站式服务能力将不断提升,海外业务进展顺利,品牌知名度也将提升,这些有助于 获取新订单。
股权激励计划将增强管理层积极性
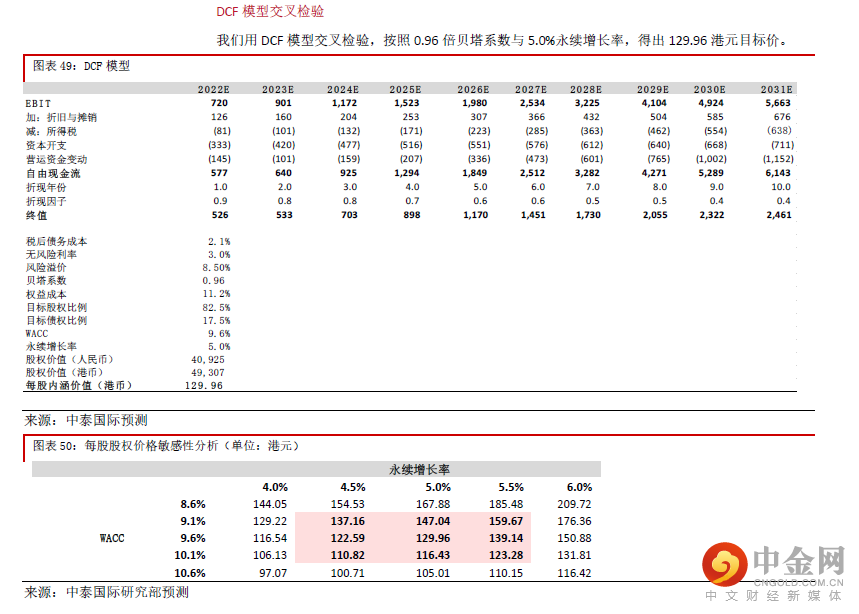
公司9 月21 日公布以83.97 人民币的授予价格向505 名业务骨干授予限制性股票,授予 价格较A 股前一个交易日收市价折让50%,我们认为大规模发行股权激励计划将提振管 理层积极性,长远看对公司发展有利。首次覆盖并给予“买入”评级,目标价131.48 港元 考虑到公司收购Biomere 后管理费用率略微上升,而且预计疫情舒缓后实验猴价格再大 幅上升的可能性不高,生物资产公允值收益将减少,预计2020-23E 股东净利润CAGR 为 36.7%,增速快于行业平均。目前股价对应53.6 倍2022E PER,低于港股行业平均的65.0 倍,估值有提升空间。目标价131.48 港元,对应64.5 倍2022E PER,给予“买入”评级。风险提示:(一)新冠肺炎全球蔓延可能对公司及客户带来影响;(二)动物实验模型 的价格涨幅如超预期可能影响业绩;(三)海外业务扩张与临床业务拓展可能慢于预期
国内领先的药物安全评价细分行业龙头
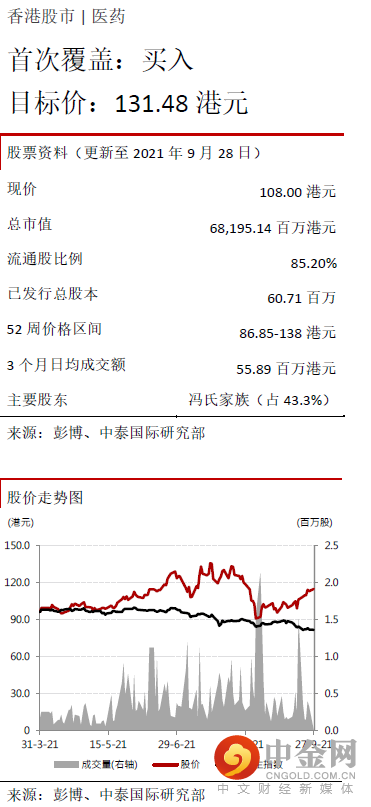
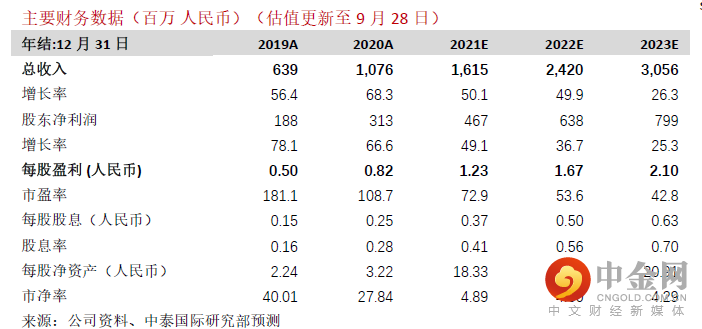
公司在国内药物安全评价领域市场份额绝对领先公司成立于1995 年,是国内领先的专门从事新药药理毒理学评价并取得卓越成就的合同研究组织。公司业 务包括非临床研究服务、临床试验与销售实验模型,其中非临床研究服务为主营业务。公司的非临床研究 服务以药物安全性评价为主,其他还涵盖药代动力学与药理及药效学研究。根据Frost&Sullivan 报告,按照 2019 年收益计算,公司是国内最大的先药物非临床安全性评价外包服务提供商,国内市场份额高达15.7%, 显著高于排名第二公司的9.9%。
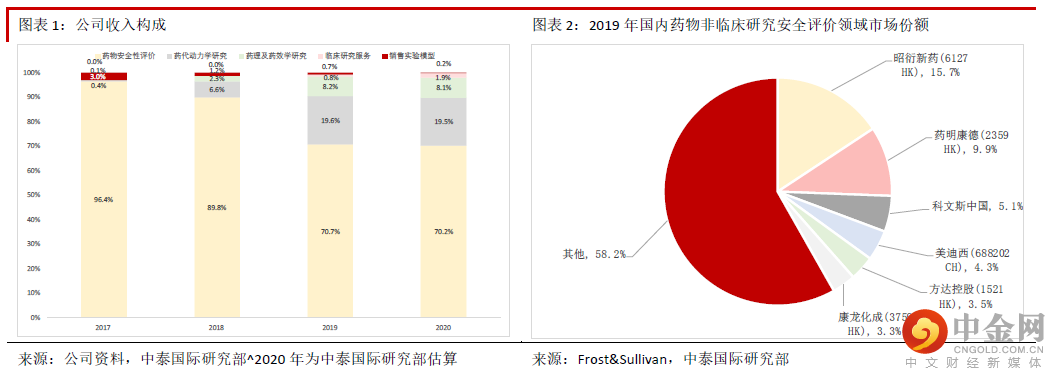
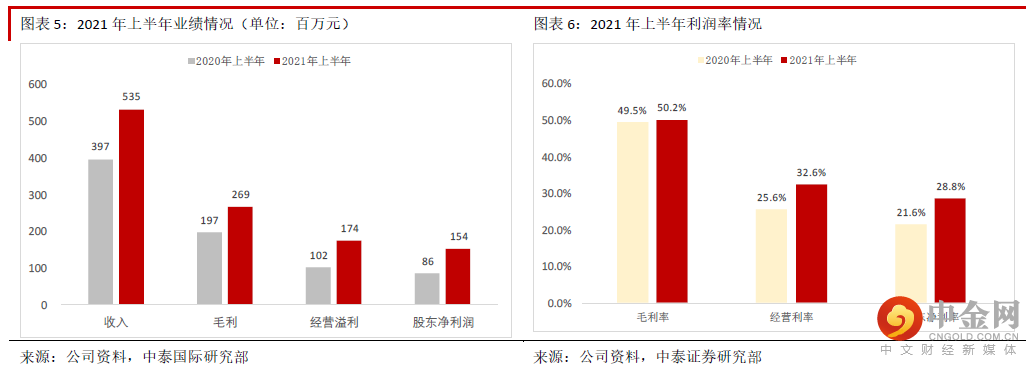
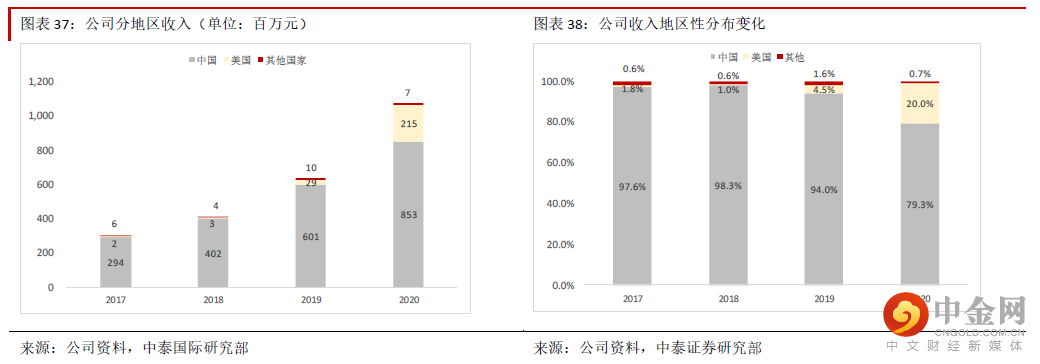
财务状况健康,业绩能见度很高公司近年来业绩持续快速增长 公司近年来获得订单的能力不断增强,原主营业务药物安全性评价收入持 续快速增长,其他新业务药代动力学、药效学研究、临床试验服务等也开始起步,因此2017-20 年收入 CAGR 增速高达52.9%。虽然近年来实验猴的价格上涨,但是公司在成本管控上较好,2018-20 年毛利率保 持稳定,而2020 年疫情期间有效控制了销售费用,导致股东净利润持续快速增长,2017-20 年股东净利润 CAGR 高达57.6%。2021 年上半年营业收入同比增长34.5%至约5.3 亿元,毛利同比增长36.5%至2.7 亿元,股东净利润同比增 长78.8%至1.5 亿元,收入与利润保持快速增长,而且公司在销售费用的管控方面非常成功,导致股东净利 润的增速快于收入。公司2021 年上半年新增订单情况非常理想,国内获得的订单同比增长55%至12 亿元, 另外通过美国Biomere 签订获得的海外订单同比增长超60%至约2,150 万美元。
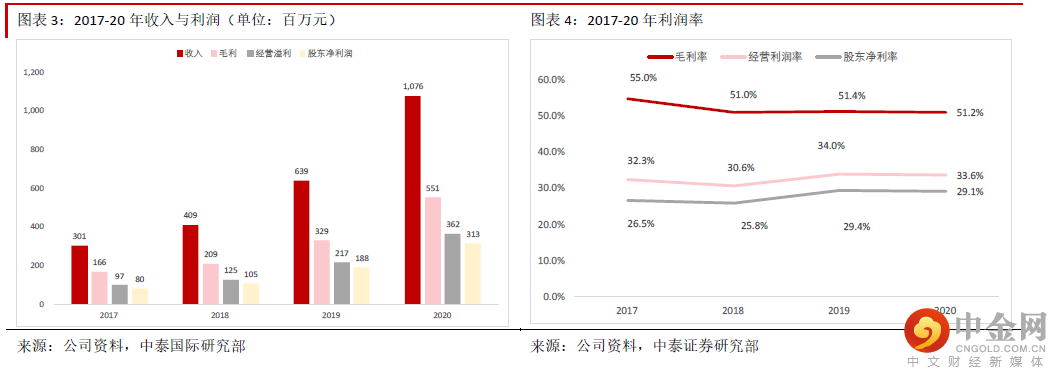
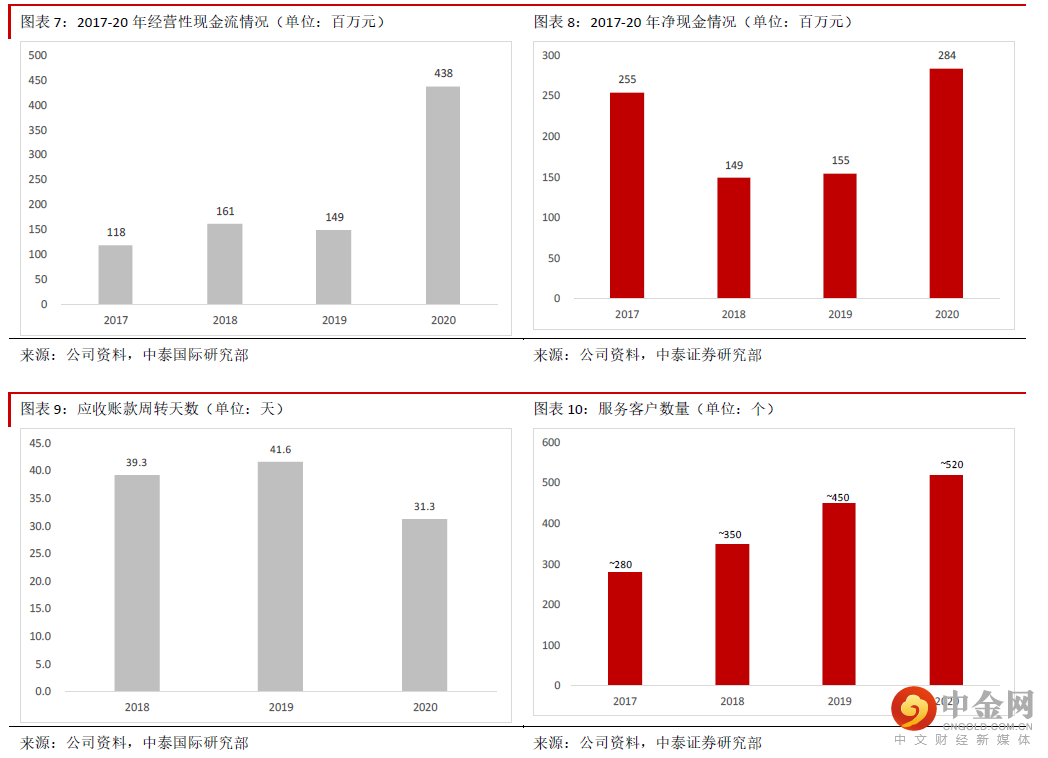
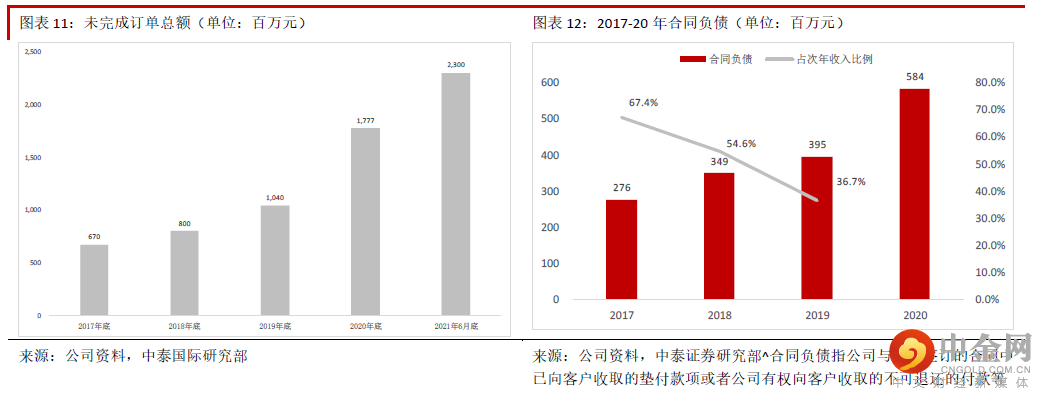
财务状况健康,未来业绩能见度高。公司过去几年财务状况良好,2020 年底银行借款金额仅约2,446 万元, 2018-20 年净现金金额持续快速增长,2020 年应收账款周转天数在缩短,经营性现金流大幅增加,表明公 司在疫情期间客户回款情况很好,财务状况健康。通常来说,我们可以用客户数量、在手订单数量变化、新增订单的情况及合同负债等先行指标预判公司的 业绩。公司客户数量从2017 年的约280 个增加到2020 年底的约520 个。公司未完成订单总额从2017 年的 约6.7 亿元增加到2021 年6 月底的约23 亿元。公司获取订单的能力越来越强,2021 年上半年新获订单约 13 亿元,接近2020 年全年的约17 亿元。我们估计2020 年获取的订单多数将在2021 年确认收入,而21 年 新获得的订单多数也将在1~2 年内完成,因此业绩能见度很高。公司的合同负债近年也快速增长,表明短 期内业绩增长性能见度很高。
药物安全性评价服务需求广阔
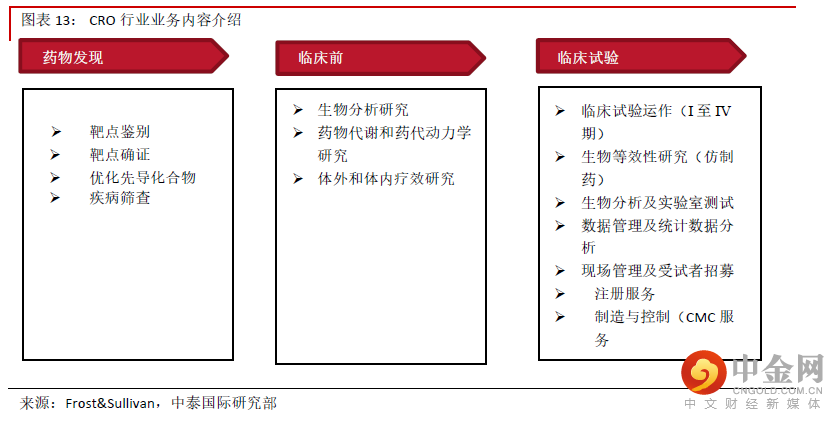
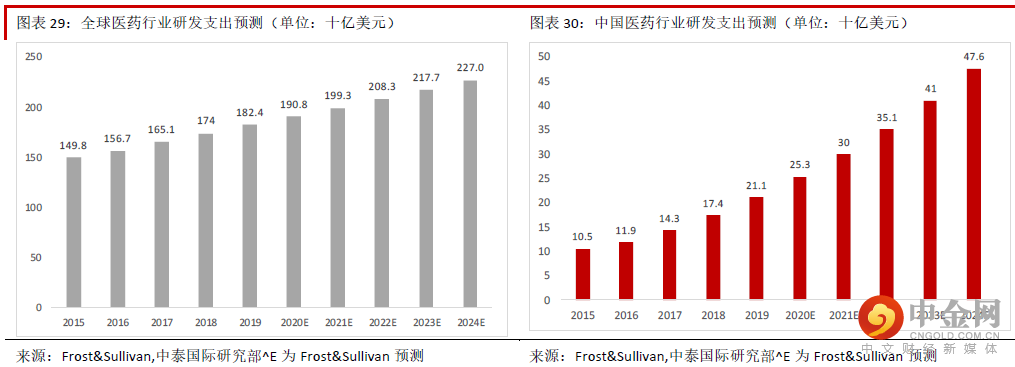
药物安全性评价是医药研发外包行业重要组成部分。公司主营业务非临床研发服务(占2020 年收入的 97.8%)主要包括药物安全性评价、药代动力学研究与临床试验服务,其中药物安全性评价是该板块的主要 业务,管理层表示约占该板块2020 年收入的70%。药物安全评价是指通过实验室研究和动物体外系统对治疗药物的安全性进行评估,是新药进入临床试验和 批准前的必要程序和重要步骤。由于很多中小型药企缺乏安评业务所需的GLP 实验室,药物安评行业的外 包率很高。根据美国行业龙头查尔斯河(CRL US)的资料,全球药物安评业务的外包率超55%。根据 Frost&Sullivan 报告,药物安全性评价是全球及中国医药研发外包行业(CRO)市场规模的6.1%及7.7%,是 CRO 行业的重要组成部分。近年来中国与全球非临床安全评价的需求快速增长。根据Frost&Sullivan 报告,该行业中国市场规模从2015 年的1.4 亿美元增加到2019 年的4.2 亿美元,2015-19 年CAGR 高达31.7%,全球市场规模从2015 年的34 亿美元增加到48 亿美元,2015-19 年CAGR 也达到9.4%。
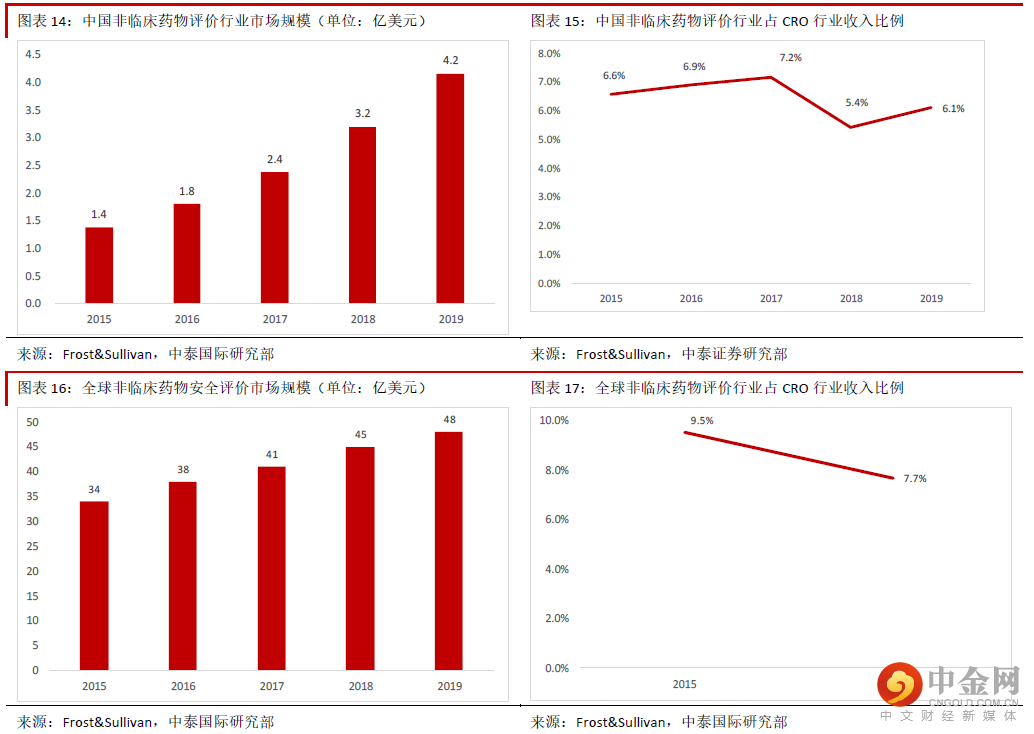
中国药物安评行业需求空间巨大。我们认为药物安全性评价未来的需求空间仍将保持快速增长,主要理由 包括:1)CRO 行业需求将持续快速增长:全球新药研发需求不断增加,中国药企也将越来越重视改良型 新药(Me-better)与创新药(First-in-class)的研发,这些将增加研发服务的需求。首先,中国市场对优质 改良型新药的需求很大。改良型新药是指在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途 径、适应症等进行优化,且具有明显临床优势,境内外均未上市的药物。由于改良型新药相对售价较低, 而且药企投入的成本与资金也不会太多,未来几年研发需求仍然会很大。其次,中国市场对优质创新药的 需求将快速增长。通常来说,优质创新药在药物靶点、分子实体、药物结构方面都有所突破,因此全球范 围内创新药的市场需求不断提升,海外龙头药企都非常注重优质创新药的研发。中国市场目前创新药占比 还明显低于全球水平,我们预计随着收入水平的提升,中国患者对优质新药的需求将增加,企业也将更加 重视创新药的研发,研发与生产外包的需求也将相应增加。2)药物安全评价的外包率将维持在高水平, 未来继续受益于医药研发需求的提升。由于中小型药企短期内很难建设GLP 实验室,我们认为未来药物安 评业务的外包率仍然会很高,将受益于新药研发的需求。3)长远看我们预计更多海外企业将使用中国药 物安全评价服务的龙头企业。中国CRO 行业的服务成本远远低于发达国家。根据上海医学临床研究中心的 统计,中国毒理服务的平均成本仅为发达国家的30%左右,因此我们预计随着国内服务水平的提升,长远 看将有更多海外药企选择中国龙头企业作为服务提供商。
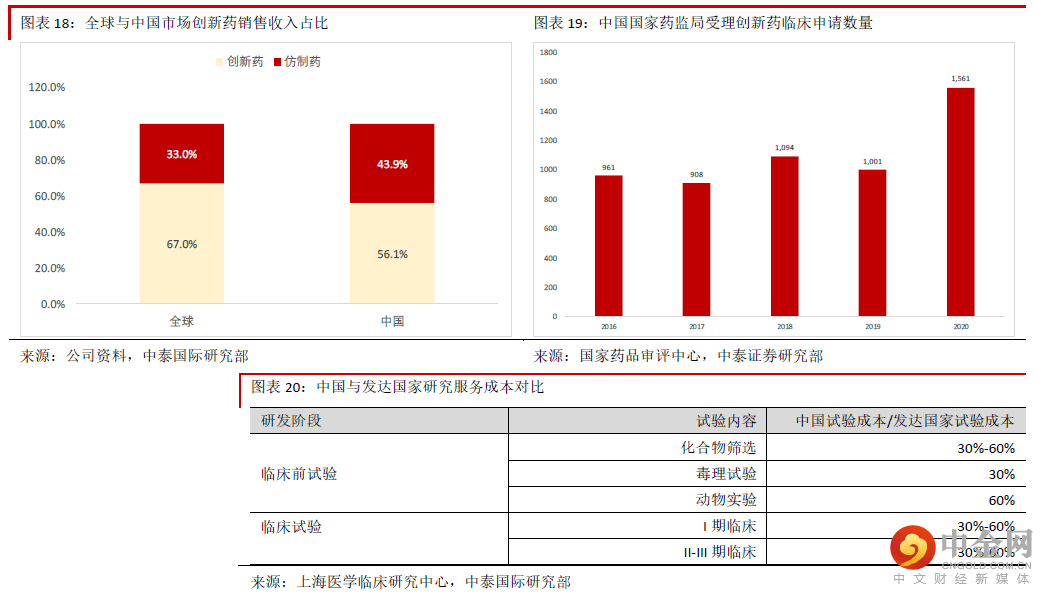
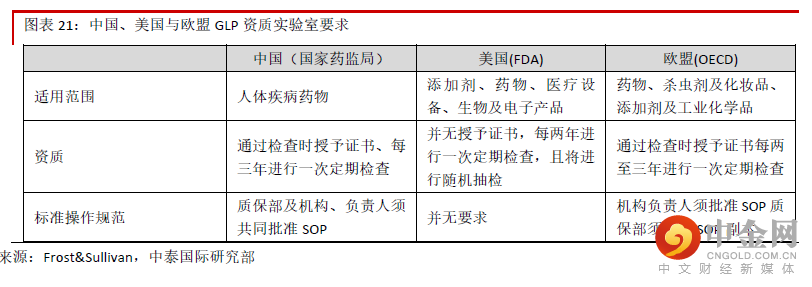
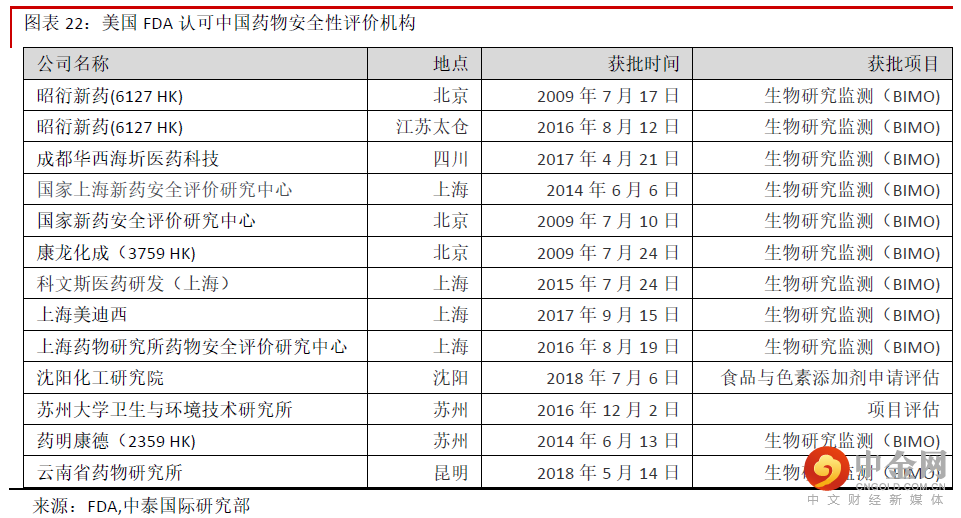
药物安全性评价服务行业壁垒很高,中小企业难以进入通常来说,药物研究所应具备GLP 认证。GLP 认证要求实验室有严格的硬件和软件设施,要具备合乎规范 的试验环境和检测设备,同时还要配备高素质的药检人才,因此建设成本通常较高。我们估计截止2017 年 6 月30 日昭衍新药在苏州拥有的19 栋动物实验楼的平均建设成本为约2,399 万元。建设动物实验楼除了土 建还需要净化装修、动物房设施建设、环境监测等工序,因此通常需要几年的时间,因此行业壁垒很高, 中小型企业很难进入。截止2017 年昭衍新药在苏州的19 栋实验楼从开工到完成环境检测投入运营的时间 为约2~7 年。公司是国内该领域的绝对龙头,从公司实验室的建设时间看, GLP 实验室建设要求很高,对 于中小企来说建设难度很高。公司作为行业龙头将率先受益于药物安评行业的需求公司是药品安全评价的行业龙头,未来将率先受益于行业需求的增加,主要原因包括:1)公司的市场份额 大幅领先于主要竞争对手,近年来每年的新增订单也快速增长,表明市场认可度很高。2)公司的实验室同 时拥有中国、经合组织(OECD)与美国食品药品监督管理局(FDA)颁发的GLP 资质,我们认为 大型药企 在选择中国的药品安全评价提供商时,将率先考虑这样的高标准公司。通常来说,OECD 与FDA 在GLP 资质 的审批方面较中国严格,目前在中国通过FDA 审评的实验室只有14 个,公司占了两个,表明实验室质量很 高。3)公司的临床实验室面积位于行业前列。对于临床前研发服务提供商来说,实验室产能非常重要,充 足的产能保证订单快速兑现。
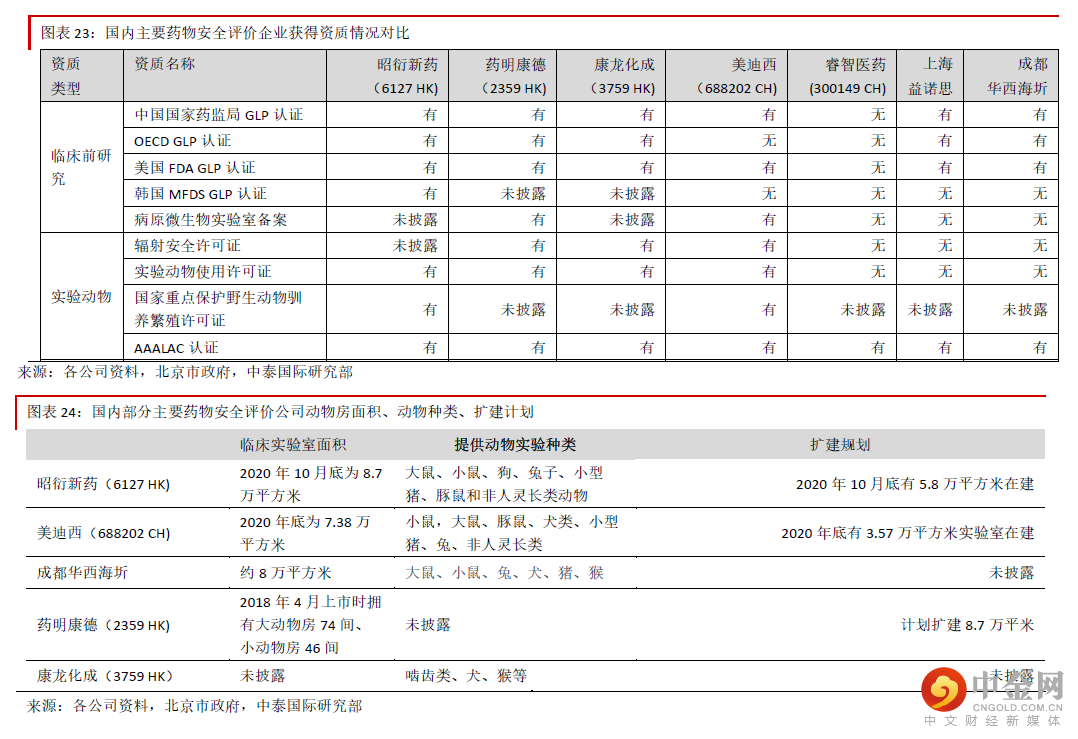
临床前后服务能力同步提升,一站式服务能力不断加强
临床前服务能力将不断提升,服务范围将不断扩大
药品安全评价业务服务能力将不断提升,新获订单将加速兑现。对于药物安评企业来说,动物实验的产能非常重要。为满足快速增长的订单需求,公司近年来不断通过翻修、新建及收购迅速扩张产能。截止2020年10月,公司总共拥有四个GLP实验室,总产能面积为约8.7万平方米。重庆与广州的试验基地目前正在建设中,建成后产能面积将增加至14.5万平方米,产能提升将帮助公司新获得的订单快速兑现。
我们估计2021年药物安评业务的收入为约7.6亿元。我们估计公司近年的新增订单中有约70%来自药物安评业务,从近年的新增订单情况推算,我们预计药物安评药物收入将维持快速增长。
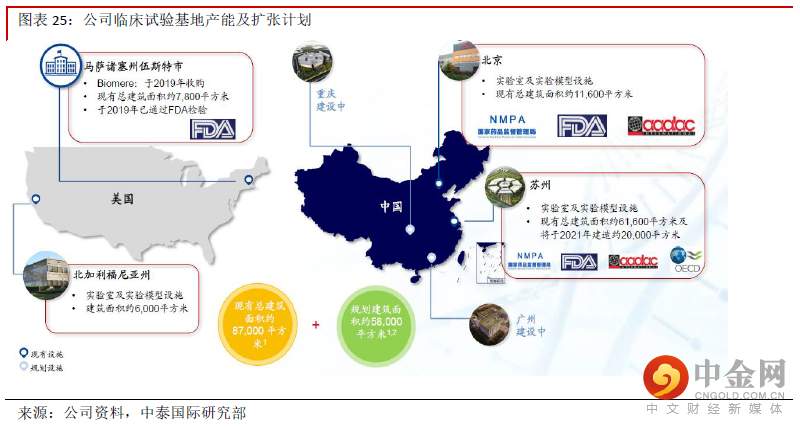
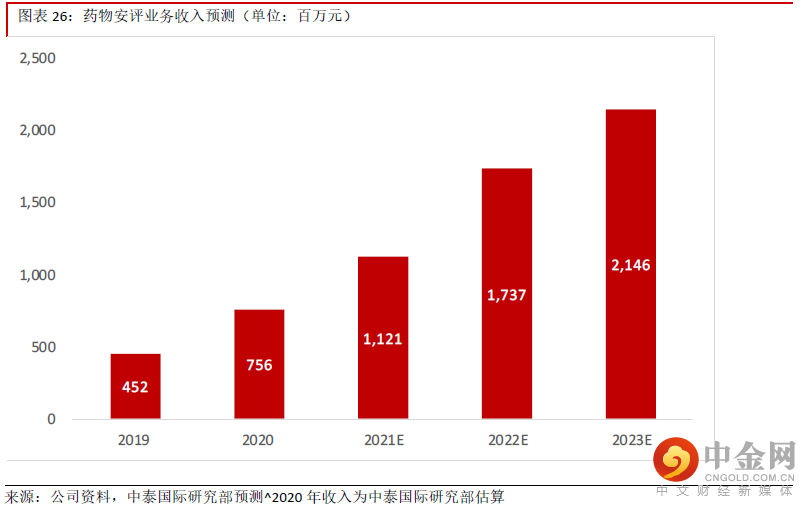
药代动力学、药效学与药理学分析方面的订单不断增加,未来将加速发展。公司的临床前研究服务除了安评以外,还包括药代动力学与药理及药效学服务。公司早年通过药物安全性评价积累了大量客户,药代动力学、药效学与药理学的订单也在不断增加,我们预计这两块业务未来将受益于行业需求的增长。
药代动力学主要包括候选药物的吸收、分布、代谢和毒性分析。公司的药代动力学研究通过自身的分析技术分析啮齿类动物、犬、小型猪和非人灵长类动物的体内药代动力学研究,测量一系列生物基质(包括血液、尿液、胆汁与组织)中的药物浓度。药代动力学除了进行药物有效性分析外,还能帮助确定新药的给药途径、给药频率与给药剂量。国内政府不断加强创新药临床试验的要求,对药物的有效性要求越来越高,而且精准医疗与个性化治疗的需求将不断提升,更多的医院将根据患者的具体情况确定给药途径、给药频率与给药剂量,而且也将更准确地为特殊人群提供特殊治疗方案,因此药代动力学研究服务的需求将不断
提升。
药效学集中在通过体内外实验研究候选药物的作用机理、量效关系、时效关系和药效特征。公司按照国内
外有关细胞治疗药物、基因治疗药物、抗体药物及其他化学药品的适用法规,进行体内外药理及药效筛选。
公司的药理及药效学研究适用范围广阔,在肿瘤学、代谢性疾病、呼吸疾病、心血管疾病、中枢神经系统等领域。公司通过提供药理及其药效学研究的服务,协助客户挑选适用于不同疾病的药物。目前来看,由于政府对新药有效性要求越来越高,药理及药效学研究的需求空间广阔。公司的药效学研究需要大量使用动物模型,公司在动物实验方面经验丰富,服务能力处于行业领先地位,因此将受益于行业需求的增长。
我们估计公司新增订单中有20%~30%来自药效学与药代动力学。从公司每年的新增订单情况可以看出,公司的药代动力学、药效学与药理学的收入将维持快速增长。我们预计2020-23E 药代动力学及药理学与药效学的收入CAGR 分别为42.6%与44.0%。
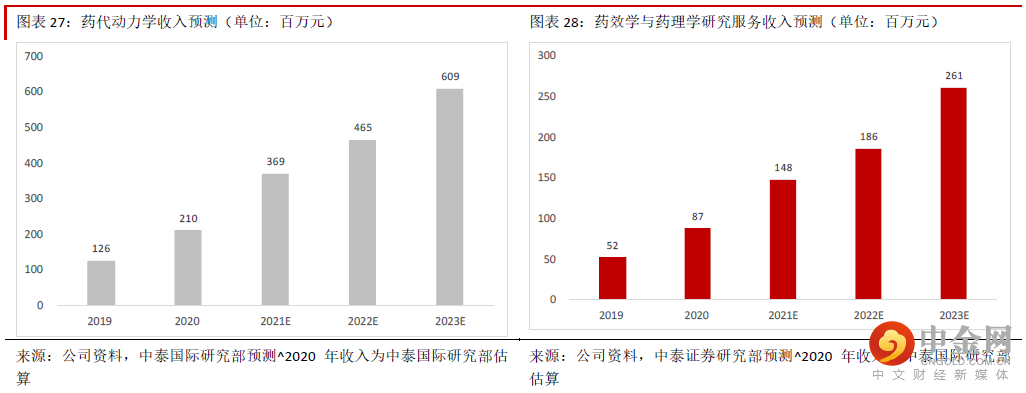
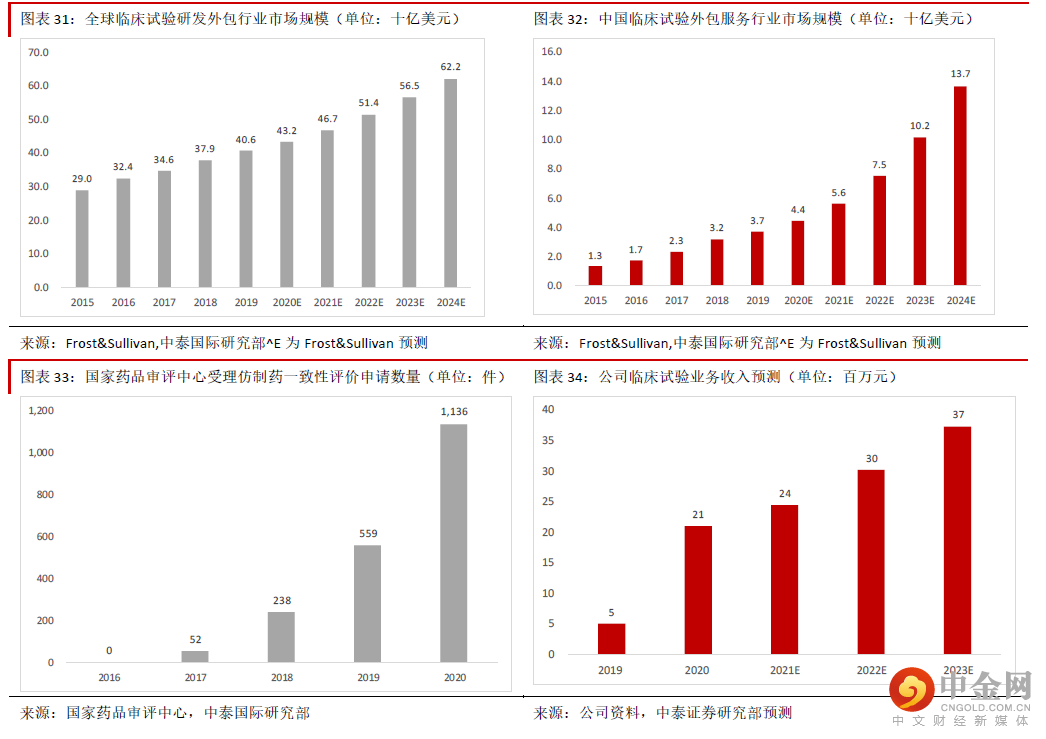
临床试验服务能力将逐步提升,一站式服务能力将不断提升公司近年开始发展临床试验领域的研发外包服务,目前主要是Ⅰ期临床与生物等效性分析为主,目前处于 起步阶段,但是近年来收入快速增长,2021 年上半年收入同比增长200.8%至约814.9 万元,我们预计未来 将快速发展,公司一站式服务能力将随之不断提升,主要原因包括:1)Ⅰ期临床试验外包服务的需求将 快速增长:优质改良型新药与创新药的需求不断提升,但是部分中小型药企缺乏临床试验的设施与科学家 资源,而CRO 行业龙头又能保证优质服务,因此临床试验的外包服务需求空间广阔。根据Frost&Sullivan 统 计,全球与中国临床试验研发外包服务市场规模的2015-19 年CAGR 分别为8.7%与29.3%,预计未来这种情 况将持续。公司目前主要从事的Ⅰ期临床是临床试验的起始部分,美国塔夫茨药物开发研究中心的论文表 明,Ⅰ期临床的费用约占临床试验总成本的22.2%,医药研发总投入的扩大必然带动Ⅰ期临床需求的增长。通常来说早期临床试验( I 期和II 期) 的外包比例较高。根据全球著名医学统计刊物PAREXEL Biopharmaceutical R&D Statistical Sourcebook(2016/17 年版)的统计,早期临床试验的外包比例为高达约 60%,因此预计随着全球创新药研发支出的增加,I 期临床试验外包的需求将快速增长。2)由于仿制药一 致性评价的推进,中国市场生物等效性研究需求空间很大。早年的中国市场由于本土药企研发能力有限, 以仿制药为主,而由于部分企业急功近利,在研发方面的投入远远少于销售推广,因此部分仿制药的疗效 与原研药差别很大。中国政府为了提升国产药物质量,2015 年起要求药企对临床试验开展自查核查工作, 为了提升仿制药品质,近年不断推进仿制药一致性评价。除此以外,政府持续推进药品带量采购,而进集 采名单的重要条件之一就是要通过一致性评价,如果不通过将无法入选,也无法获得政府的承诺采购量, 因此一致性评价的需求将持续增长。3)公司临床试验的产能在提升:公司目前总共拥有三个临床试验中 心,其中苏州太仓第一人民医院的1 期临床中心2021 年上半年投产,我们预计随着新临床中心的投产,公 司在临床试验方面承接订单的能力将持续增加,一站式服务能力将不断提升。4)订单数量将不断增加:公司通过主营业务药物安全评价业务,在CRO 领域已经建立起很好的品牌知名度。随着临床试验领域的产 能提升,我们预计将有更多的企业选择公司做临床试验阶段的研发服务提供商。公司2021 年上半年临床试 验阶段的订单金额同比增长超150%至约4,000 万元,表明公司服务的市场认可度在提升,未来这种态势将 持续。5)晚期临床业务将逐渐起步:公司的Ⅰ期临床项目将逐步向Ⅱ~Ⅲ期推进,而且随着公司在临床 试验外包服务领域的知名度不断提升,预计将有更多药企选择公司作为晚期临床试验服务提供商,这块业 务将逐渐起步。
自建动物基地长远利于提升原材料自给率
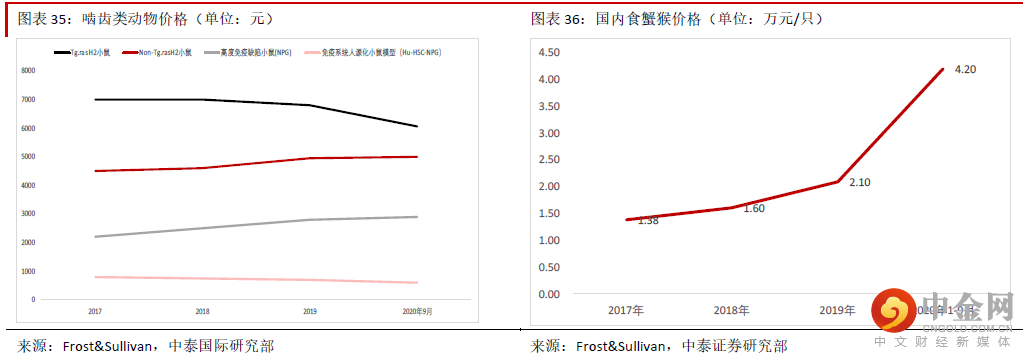
公司的服务成本主要包括直接劳工成本、物资成本(耗材与实验模型)与间接成本(折旧与摊销及水电费 等)及生物资产公平值变动调整的影响,其中物资成本占比最大,分别占2017-19 年服务成本的50.4%、 44.5%、45.3%,是影响公司毛利率的主要因素。公司的实验模型主要包括非人灵长类动物与啮齿类动物。通常来说,由于啮齿类动物(大鼠、小鼠、比格犬等)繁殖周期较短,因此供应较为充足,价格稳定有些 还下降,但是与人类同源性较强的灵长类动物价格却在上涨。由于人类过度使用自然资源,而且灵长类动 物繁殖期较长,2020 年后新冠疫情对于灵长类动物的繁殖生长也造成影响,因此供不应求情况明显。根据 Frost&Sullivan 报告,常用非人灵长类实验动物食蟹猴的均价已经从2017 年的每只约1.38 万元上涨到2020 年1-9 月的每只约4.2 万元,这些情况导致公司的毛利率2018 年以后有所下降。为了增加动物实验模型的 自给率,公司从2019 年11 月开始在广西梧州建设动物基地,截止2021 年6 月底,基地的主体工程已经竣 工,今后仅需进行装饰装修及室外工程等。管理层表示由于疫情原因投入使用略需时间,但是投入使用后 能饲养约1 万头非人灵长类动物。我们认为长远看,提升非人灵长类动物的自给率有助于控制成本。
海外市场竞争力将逐步提升
公司的服务成本主要包括直接劳工成本、物资成本(耗材与实验模型)与间接成本(折旧与摊销及水电费 等)及生物资产公平值变动调整的影响,其中物资成本占比最大,分别占2017-19 年服务成本的50.4%、 44.5%、45.3%,是影响公司毛利率的主要因素。公司的实验模型主要包括非人灵长类动物与啮齿类动物。通常来说,由于啮齿类动物(大鼠、小鼠、比格犬等)繁殖周期较短,因此供应较为充足,价格稳定有些 还下降,但是与人类同源性较强的灵长类动物价格却在上涨。由于人类过度使用自然资源,而且灵长类动 物繁殖期较长,2020 年后新冠疫情对于灵长类动物的繁殖生长也造成影响,因此供不应求情况明显。根据 Frost&Sullivan 报告,常用非人灵长类实验动物食蟹猴的均价已经从2017 年的每只约1.38 万元上涨到2020 年1-9 月的每只约4.2 万元,这些情况导致公司的毛利率2018 年以后有所下降。为了增加动物实验模型的 自给率,公司从2019 年11 月开始在广西梧州建设动物基地,截止2021 年6 月底,基地的主体工程已经竣 工,今后仅需进行装饰装修及室外工程等。管理层表示由于疫情原因投入使用略需时间,但是投入使用后 能饲养约1 万头非人灵长类动物。我们认为长远看,提升非人灵长类动物的自给率有助于控制成本。
预计2020-23E股东净利润CAGR达36.7%
预计2020-23E收入CAGR为41.6%
我们预计公司2020年获得的约17亿元订单中的大部分将于2021年完成。公司2021年上半年已经获得约13亿元订单,保守预计全年将获得23亿元订单,其中多数将在一年内年内完成。考虑到中国及全球市场新药研发的需求,我们预计2022-23年订单总额也将维持快速增长,因此预计2020-23E收入CAGR为41.6%。
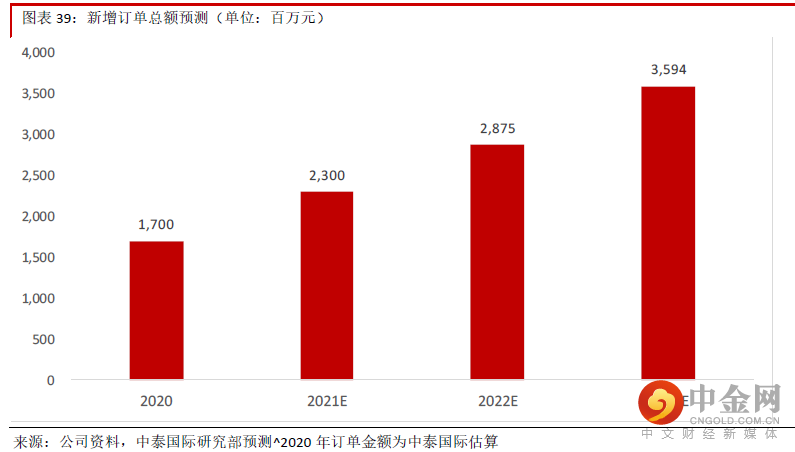
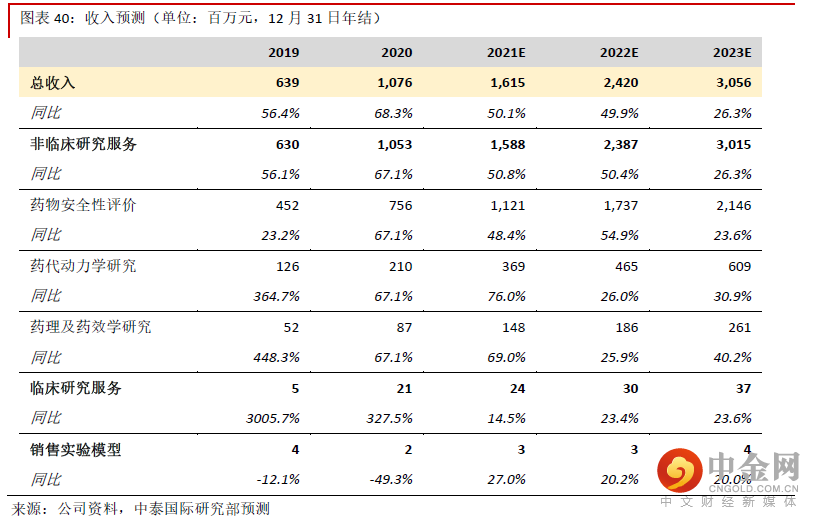
预计2020-23E股东净利润CAGR达36.7%
公司近年在生产成本控制方面很成功,2018-20年毛利率稳定,我们预计未来这种情况将持续。由于2020-2021年公司的管理费用分别涵盖约1,000万元上市费用,而且公司收购的美国公司Biomere的管理费用率较公司原有业务略高,因此预计2020年后管理费用率略高于以往。我们认为随着疫情的舒缓,实验猴价格再大幅上升的可能性不高,2022年后生物资产公允值收益将下降,经营利率与股东净利率将略微下降,但是总体来看公司股东净利润的2020-23E CAGR仍将达到36.7%的高水平。公司股东净利润将从2020年的3.1亿元增加至2023年的约8.0亿元,而2021-23E股东净利率将高达28.9%、26.3%、26.1%。
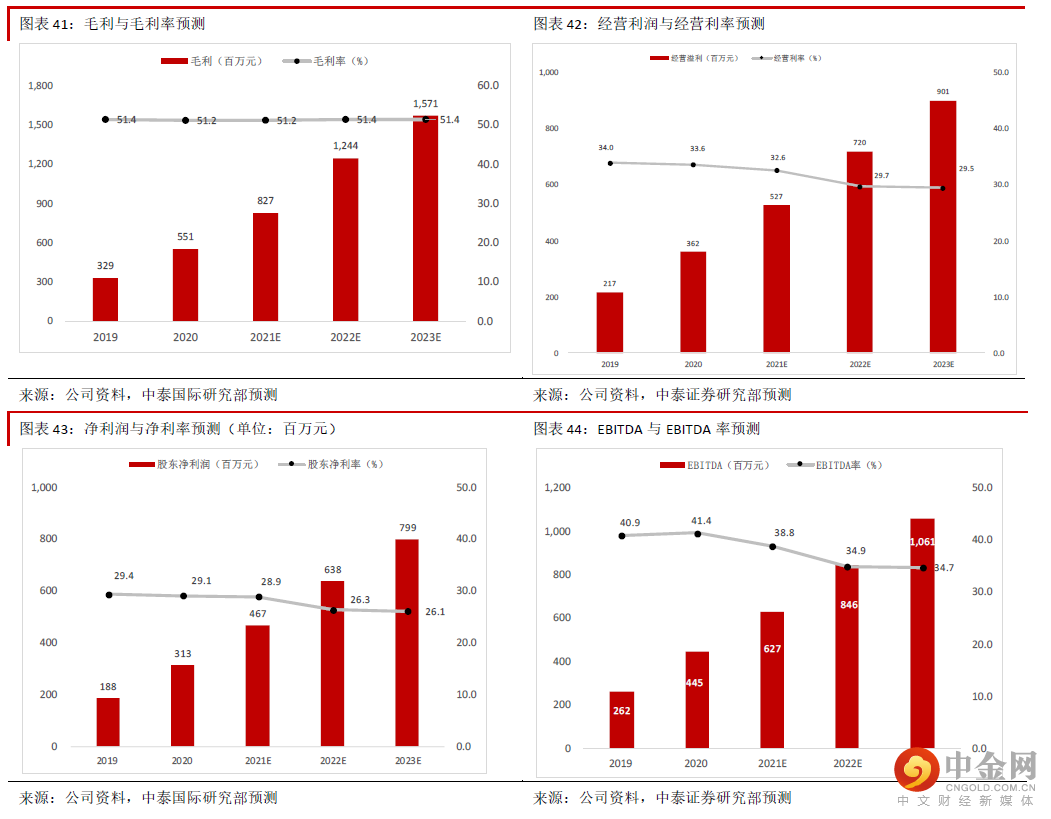
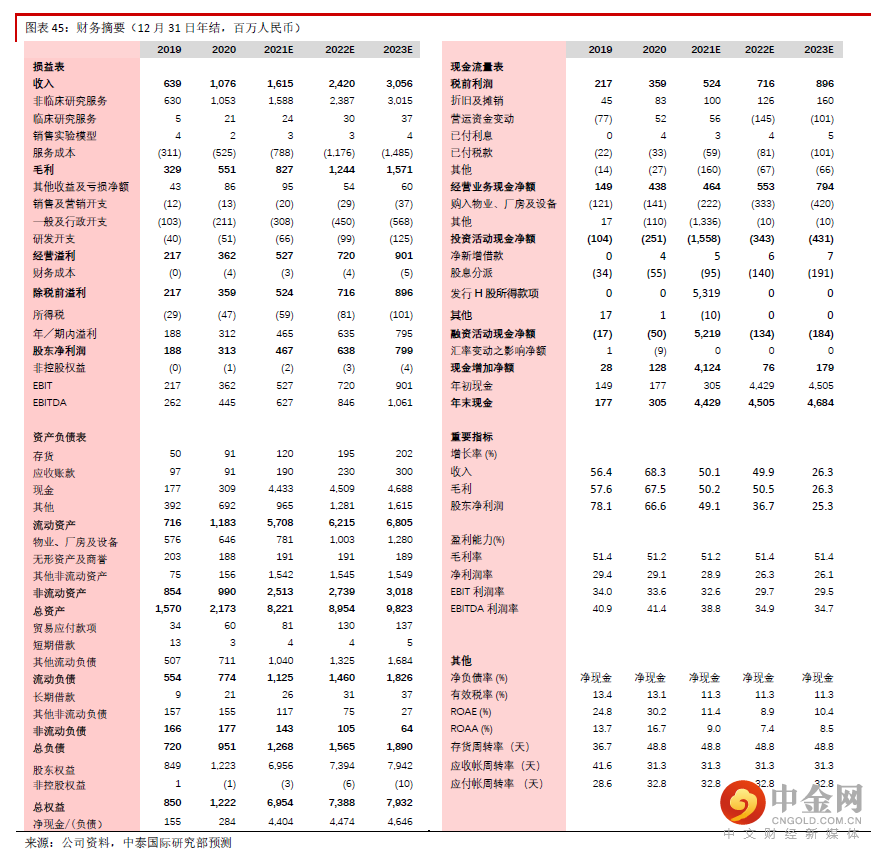
给予“买入”评级,目标价131.48 港元
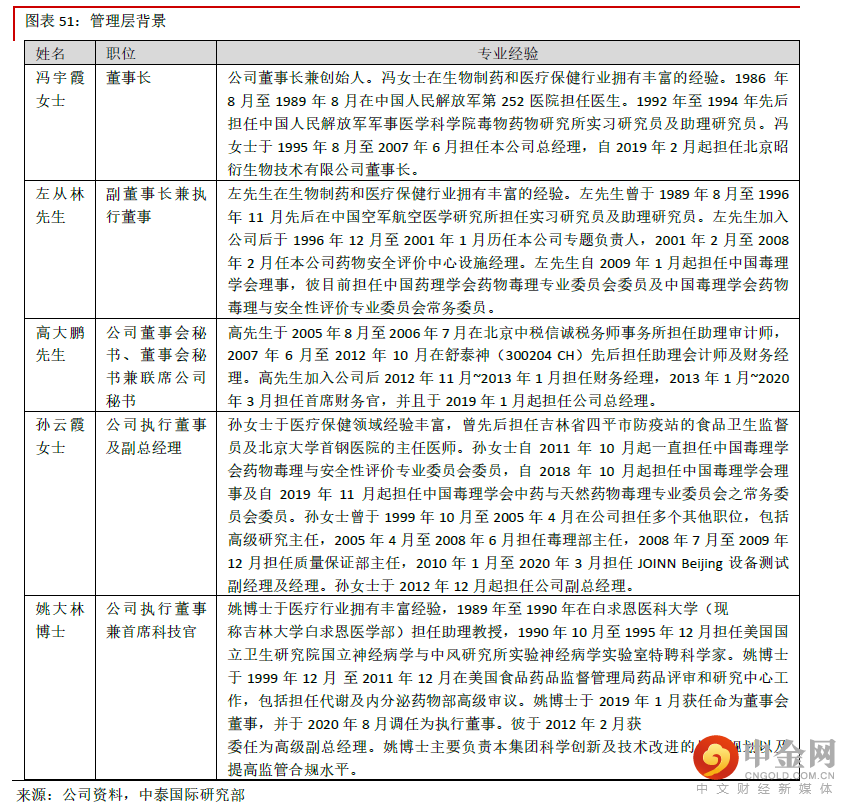
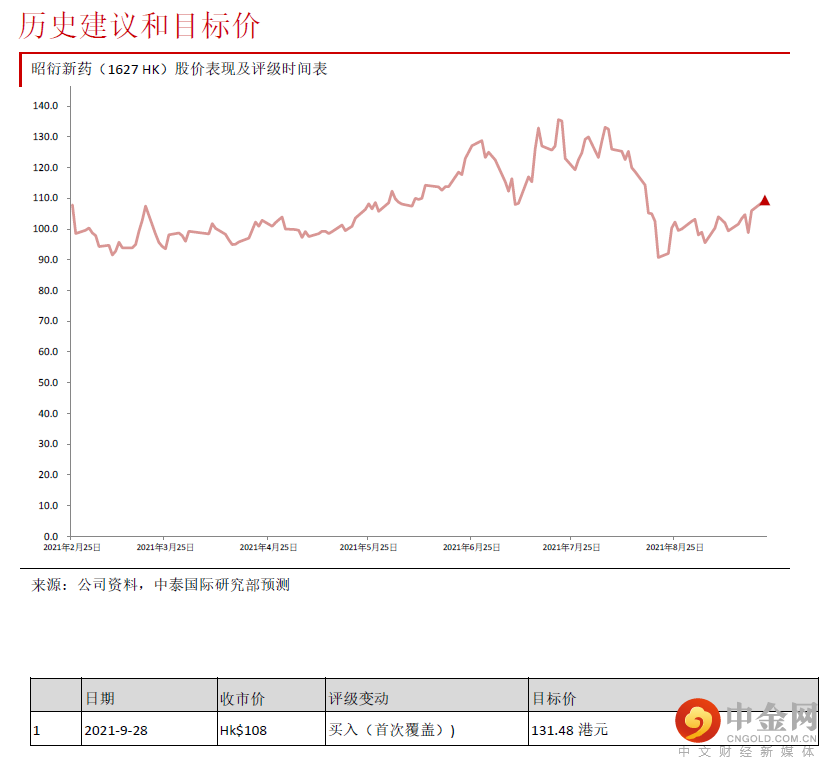
考虑到港股医药生产与外包服务行业(CXO)行业在香港市场标的已经较多,而且公司业绩前瞻性很强, 现金流稳定,我们用DCF 模型做交叉检测,平均得出131.48 港元的目标价,给予“买入”评级。相对估值法估值我们选取港股医药研发与生产外包服务(CXO)板块的药明生物(2269 HK)、药明康德(2359 HK)、泰格 医药(3347 HK)、康龙化成(3759 HK)、方达控股(1521 HK)做比较,同时也参考A 股中与公司同样主 要从事临床前研发服务企业美迪西(688202 CH)、成都先导(688222 CH)的情况,A 股公司中美迪西在 2019 年国内药物安评领域排名第四(见图表2),是公司主要竞争对手之一。公司目前股价对应53.6 倍2022E PER,显著低于香港上市同业平均的66.4 倍,较A 股主要竞争对手折让更 大。公司与药明生物(2269 HK)、药明康德(2359 HK)、康龙化成(3759 HK)等提供一站式服务的龙头 企业相比,目前业务主要集中于药物安评这个板块,高毛利的后期临床业务与商业生产业务还有待扩充, 但是药物安评是研发外包服务中外包率最高的板块,因此市场需求非常大,而且公司是国内这个板块绝对 龙头,而且产业链在不断扩充,因此收入与股东净利润均将维持快速增长。我们预计公司2020-23E 股东净 利润的CAGR 为36.7%,快于行业平均的33.7%,我们认为公司估值有提升空间,按照相对估值法估值,用 66 倍2022E PER 估值,得出133.0 港元目标价